Anvisa autoriza testes clínicos de mais duas vacinas contra a Covid-19 no Brasil
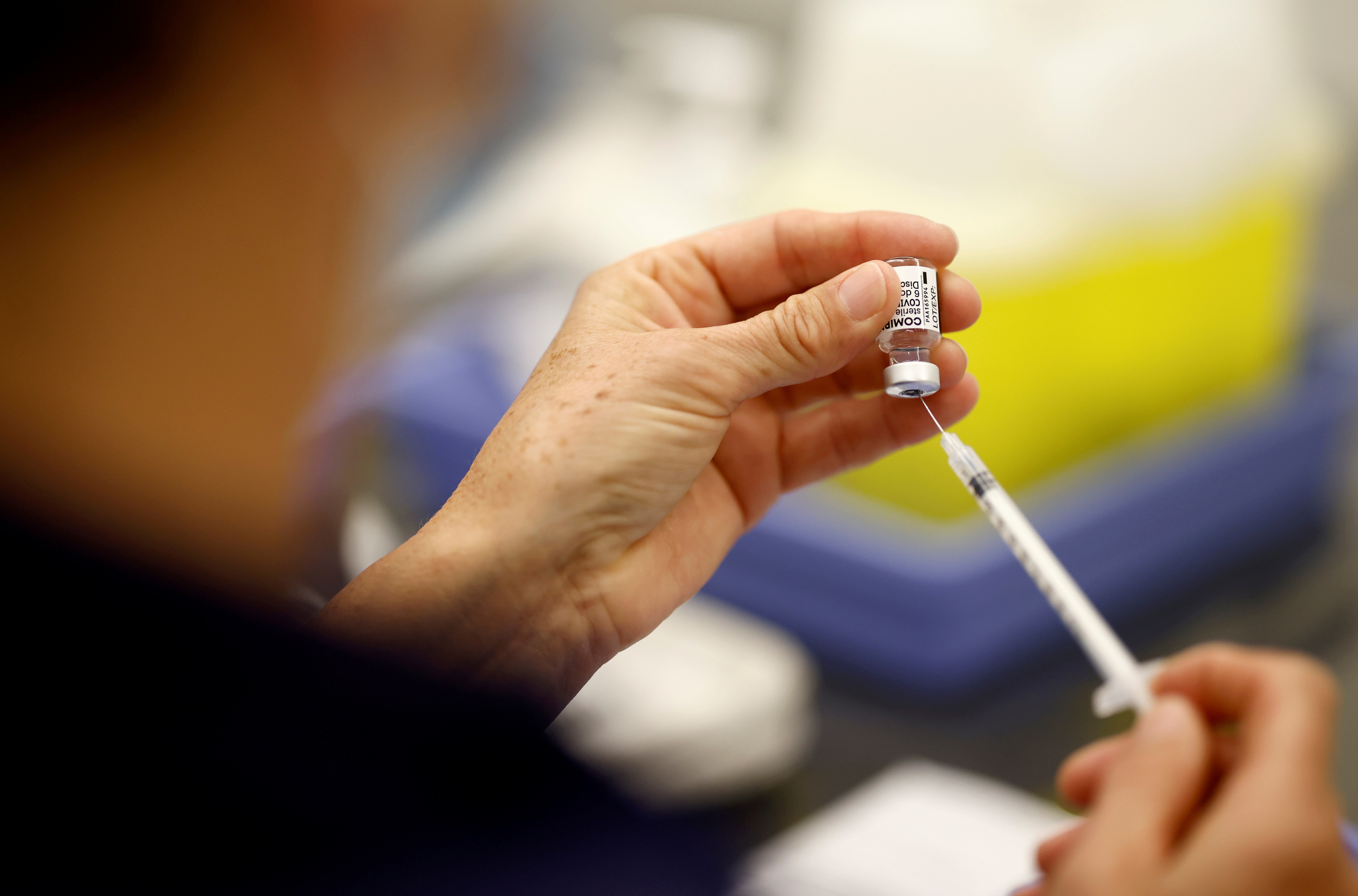
Uma das vacinas é uma nova versão da AstraZeneca, modificada para também fornecer imunidade contra a variante beta. A outra candidata é uma vacina inativada desenvolvida na China. Ensaios serão feitos em 9 estados ao todo. Ao todo, dez testes clínicos foram autorizados no Brasil. Dose de vacina da Pfizer/BioNTech sendo preparada em Saint-Nazaire, França, em 28 de maio
Stephane Mahe/Arquivo/Reuters
A Agência Nacional de Vigilância Sanitária (Anvisa) autorizou, nesta quarta-feira (14), testes clínicos de mais duas vacinas contra a Covid-19 no Brasil.
Uma delas é uma nova versão da vacina de Oxford/AstraZeneca, modificada para também fornecer imunidade contra a variante beta. A segunda vacina é inativada, desenvolvida pelo Instituto de Biologia Médica da Academia Chinesa de Ciências Médicas, em Pequim, na China.
Os novos ensaios serão feitos em 9 estados ao todo (veja detalhes mais abaixo), com 8.792 voluntários.
Com as duas aprovações, o país passa a ter 10 pesquisas clínicas de vacina aprovadas desde o início da pandemia (veja lista ao final desta reportagem).
Veja, abaixo, detalhes sobre as vacinas que serão testadas:
Vacina AZD2816
A vacina AZD2816, uma versão modificada da AstraZeneca, vai usar a mesma tecnologia da anterior (vetor viral). A nova vacina foi modificada para também fornecer imunidade contra a variante beta – contra a qual a primeira versão deu apenas proteção limitada.
USP confirma variante sul-africana do coronavírus em amostra de paciente de Sorocaba
Infográfico mostra como funcionam vacinas de vetor viral contra o coronavírus
Anderson Cattai/G1
A pesquisa será feita na Bahia, no Distrito Federal, no Paraná, no Rio Grande do Norte, no Rio Grande do Sul e em São Paulo. Serão 800 voluntários. Poderão participar pessoas já vacinadas e também as que ainda não receberam uma vacina contra a Covid.
Como serão os testes?
Poderão participar adultos de 18 anos ou mais. O estudo será de fase 2 e 3 simultâneas e vai testar a segurança e a imunogenicidade da vacina – capacidade dela de induzir uma resposta do sistema de defesa do corpo.
A medida da resposta imune será feita comparando 3 situações de aplicação da vacina:
Quando ela é dada em dose única a pessoas que não têm anticorpos contra o coronavírus, mesmo depois de vacinadas. Os testes serão feitos em quem recebeu as duas doses da primeira vacina da AstraZeneca (que está sendo aplicada no Brasil) ou de uma vacina de RNA mensageiro (no Brasil, apenas a da Pfizer está sendo aplicada).
Quando ela é dada em 2 doses a pessoas que não têm anticorpos contra o coronavírus e que não foram vacinadas.
Quando ela é dada apenas como segunda dose para quem receber a primeira vacina da AstraZeneca na primeira dose. Nesse caso, as pessoas não podem ter anticorpos para o vírus, e também não poderão ter sido vacinadas antes dos testes.
Nos casos em que os voluntários deverão estar vacinados antes dos ensaios, a segunda dose deve ter sido recebida pelo menos 3 meses antes da primeira aplicação de vacina do estudo.
Os testes também serão feitos no Reino Unido, África do Sul e Polônia. Ao todo, incluindo os voluntários do Brasil, 2.475 pessoas participarão dos ensaios.
Vacina da Academia Chinesa de Ciências Médicas
A outra vacina autorizada para testes é inativada (como a CoronaVac), desenvolvida pela Academia Chinesa de Ciências Médicas.
Infográfico mostra como funcionam vacinas inativadas contra o coronavírus
Anderson Cattai/G1
A pesquisa será feita nos estados de Goiás, Rio de Janeiro, Santa Catarina e São Paulo, com 7.992 participantes ao todo. Todos precisam ter 18 anos ou mais.
Como serão os testes?
O teste será de fase 3, com grupo placebo (que recebe uma substância inativa para medir os efeitos) para avaliar a eficácia, segurança e a imunogenicidade da vacina. Serão duas doses, aplicadas com intervalo de 14 dias entre a primeira e segunda dose.
Os testes também serão feitos na Malásia, em Bangladesh, na China e no México. Ao todo, cerca de 34.020 pessoas participarão dos ensaios.
Vacinas testadas no Brasil
As vacinas aprovadas para estudos anteriormente foram:
2 de junho de 2020: Oxford/AstraZeneca (concluído/está sendo aplicada no Brasil)
3 de julho de 2020: CoronaVac (concluído/está sendo aplicada no Brasil)
21 de julho de 2020: vacina da Pfizer/BioNTech (concluído/está sendo aplicada no Brasil)
18 de agosto de 2020: a vacina da Janssen-Cilag/Johnson (concluído/está sendo aplicada no Brasil)
8 de abril de 2021: vacina da Medicago/GSK (fase 3)
16 de abril de 2021: vacina da Sichuan Clover Biopharmaceuticals, a SCB-2019 (fase 3)
13 de maio de 2021: Covaxin (fase 3)
6 de julho de 2021: Sanofi (fases 1/2)
As vacinas da Pfizer/BioNTech e da AstraZeneca/Oxford já obtiveram registro definitivo de uso junto à Anvisa. Já a CoronaVac e a vacina da Johnson/Janssen têm autorização para uso emergencial.
Atualmente, o Plano Nacional de Imunização (PNI) usa quatro vacinas na população brasileira: CoronaVac, Oxford, Pfizer e Johnson.
Tire dúvidas com VÍDEOS sobre as vacinas de Covid-19:





